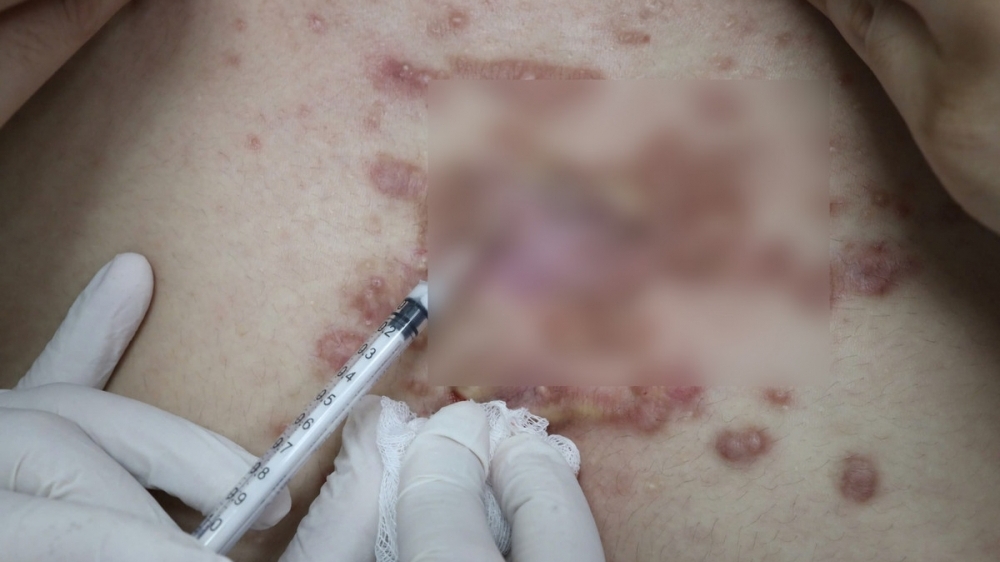
Lỗ hổng trang thiết bị y tế: Phân loại "lạ" vẫn lọt cửa kiểm soát của cơ quan chức năng
Dù được quảng cáo có các thành phần dược liệu với khả năng tan, thẩm thấu thậm chí có sản phẩm còn được hướng dẫn đặt trong cơ thể 3 ngày nhưng vẫn được phân loại là trang thiết bị y tế loại A. Theo Quy định thì trang thiết bị y tế loại A là những sản phẩm có mức độ rủi ro thấp và chỉ được tồn tại trong cơ thể ở thời gian tạm thời (khoảng 60 phút).
Đơn cử như cùng một chủng loại sản phẩm là Viên đặt phụ khoa được phân loại dựa trên quy tắc 5 nhưng Trung tâm Dịch vụ Kỹ thuật Thiết bị Y tế - trường Cao đẳng kỹ thuật thiết bị y tế đã xếp nhiều sản phẩm ở mức độ rủi ro thấp (thiết bị y tế loại A) và có sản phẩm lại được xếp loại rủi ro cao hơn (loại B).
 |
| Mẫu nhãn được đăng ký lưu hành của sản phẩm Viên đặt phụ khoa Nữ oa |
Các sản phẩm được Trung tâm này phân loại là trang thiết bị y tế loại A gồm: Viên đặt phụ khoa Nữ Oa; Viên đặt phụ khoa Vương Nữ Xuân; Kén đặt phụ khoa Kim Nữ, Viên đặt phụ khoa Hồng Quý Phi, Viên đặt phụ khoa Nhất Nhất, Viên đặt phụ khoa Thanh Cung Bảo, Viên đặt phụ khoa S1, Viên đặt phụ khoa Thảo Nguyên...Đặc điểm chung của các sản phẩm này đều là được sản xuất trong nước có sử dụng thành phần là dược liệu và được mô tả có công dụng se khít âm đạo, làm hồng âm đạo... dùng trong các trường hợp viêm nhiễm phụ khoa.
 |
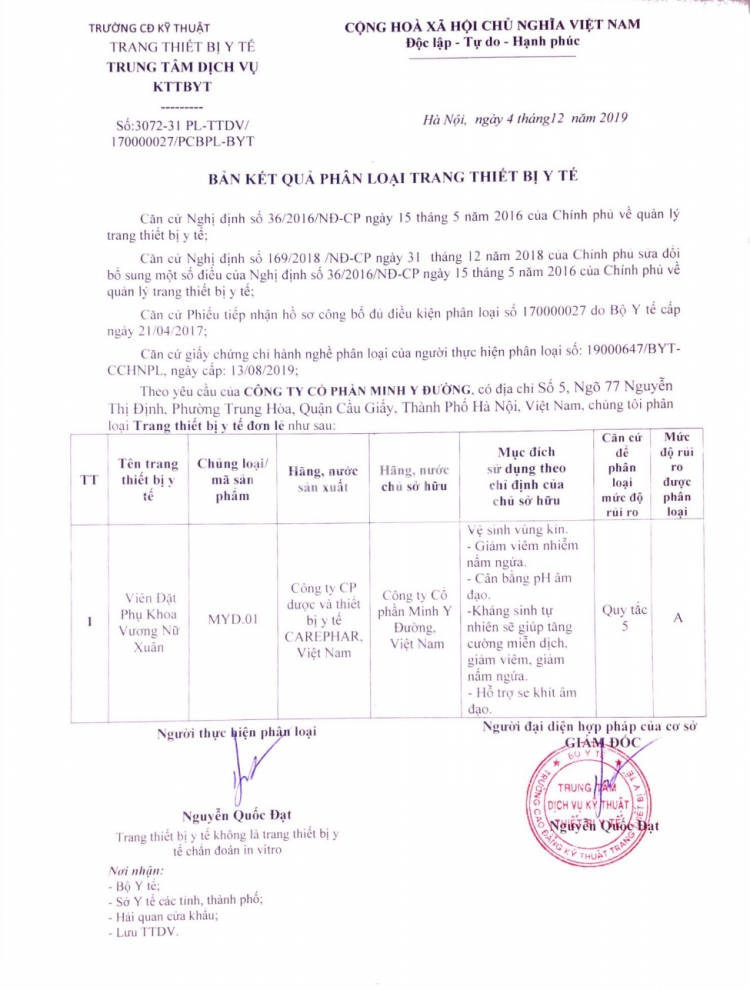
| Mẫu nhãn của sản phẩm Viên đặt phụ khoa Vương Nữ Xuân |
Trong khi đó cùng là dòng sản phẩm Viên đặt âm đạo nhưng có xuất xứ nước ngoài thì lại được phân loại ở mức độ rủi ro cao hơn như: Viên đặt âm đạo Perregyn ovuli vaginali (loại B).
Ngoài ra, Trung tâm Dịch vụ Kỹ thuật Thiết bị Y tế còn có Công ty TNHH Dịch vụ Kỹ thuật và Thương mại Quang Minh; Công ty TNHH Khoa học Kỹ thuật và Thiết bị y tế Đức Phúc cũng phân loại các Viên đặt phụ khoa là trang thiết bị y tế loại A.
Một số sản phẩm do các công ty này phân loại gồm: Viên đặt phụ khoa Lady Charm,;Viên đặt phụ khoa Hồng Âm Lan Chi X2; Viên đặt phụ khoa họ Đinh...

Ở phần mô tả kỹ thuật trang thiết bị y tế của các sản phẩm này, chủ sở hữu sản phẩm đưa ra những thông tin sử dụng của các sản phẩm như một loại thuốc điều trị với các thành phần dược liệu được bào chế dạng viên, dạng kén và hướng dẫn sử dụng như: “Phải nằm yên ít nhất 30 phút để viên kịp tan và ngấm đều vào niêm mạc âm đạo”; "đặt sâu viên đặt vào trong âm đạo đến 3 ngày sau mới lấy viên đặt ra và đặt viên mới".
Rõ ràng việc trang thiết bị y tế có khả năng thẩm thấu vào âm đạo như vậy thì không thể kiểm soát được thời gian sản phẩm tồn tại trong cơ thể là bao lâu và hướng dẫn đặt trong 3 ngày sau biệt hoàn toàn so với quy định về trang thiết bị y tế loại A nhưng không hiểu vì lý do gì mà các đơn vị này lại phân loại là trang thiết bị y tế có mức độ rủi ro thấp nhất (?!)
Dù kết quả phân loại có rất nhiều vấn đề cần làm rõ nhưng cơ quan y tế nhiều địa phương trong đó có sở Y tế thành phố Hà Nội, Thành Phố Hồ Chí Minh, Bắc Giang... vẫn cấp phiếu tiếp nhận. Khi được cấp phiếu tiếp nhận sản phẩm nghiễm nhiên được lưu hành dưới "vỏ bọc" là trang thiết bị y tế loại A.
Một chuyên gia y tế cho biết: “Nếu sản phẩm dùng để điều trị mà có sử dụng thành phần dược liệu thì phải được đăng ký là thuốc và phải tuân thủ các quy định thử lâm sàng nghiêm ngặt hơn”. Nhưng tại sao các sở y tế vẫn cấp phiếu tiếp nhận công bố cho những sản phẩm viên đặt phụ khoa đã nêu ở trên?

Theo quy định, một đơn vị được thực hiện phân loại trang thiết bị y tế phải kê khai đầy đủ thông tin về nhân sự và những nhân sự này phải có điều kiện chuyên môn. Dẫu vậy, trong văn bản công bố số 01-VBPL/TTDV củaTrung tâm Dịch vụ Kỹ thuật Thiết bị Y tế không có tên nhân sự Nguyễn Quốc Đạt nhưng tại một số bản kết quả phân loại trang thiết bị y tế lại thể hiện tên người thực hiện phân loại là: Nguyễn Quốc Đạt (?!)
 |
| Trong văn bản công bố số 01-VBPL/TTDV của Trung tâm Dịch vụ Kỹ thuật Thiết bị Y tế không đề cập đến tên Nguyễn Quốc Đạt |
Việc cấp phiếu tiếp nhận trang thiết bị y tế giống như cấp phiếu công bố cho thực phẩm chức năng là theo nguyên tắc hậu kiểm nhưng vẫn phải dựa trên hồ sơ công bố trong đó có kết quả phân loại. Nhưng những hồ sơ công bố có tài liệu phân loại dùng các từ như "thuốc" "điều trị"... để mô tả sản phẩm mà vẫn được các cơ quan chức năng cấp phiếu tiếp nhận trang thiết bị y tế.
Phải chăng đây là "điểm mù" trong bộ hồ sơ công bố của sản phẩm nên mới dễ dàng lọt qua cửa kiểm duyệt của các cơ quan chức năng?
(Còn tiếp...)