Hội đồng Đạo đức đã thông qua kết quả thử nghiệm vắc xin Nanocovax
GS.TS Trương Việt Dũng, Chủ tịch Hội đồng Đạo đức trong nghiên cứu y sinh học quốc gia (Bộ Y tế) cho biết Hội đồng đã chấp thuận kết quả thử nghiệm lâm sàng giữa kỳ pha 3a vắc xin Nanocovax của Công ty Nanogen. Hiện hồ sơ, dữ liệu đã được chuyển sang Hội đồng Tư vấn cấp giấy đăng ký lưu hành thuốc, nguyên liệu làm thuốc của Bộ Y tế để xem xét cấp phép khẩn cấp có điều kiện.
 |
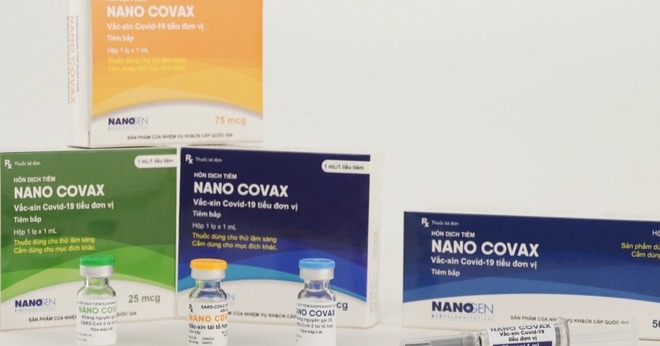
| Vắc xin Nanocovax do Công ty Nanogen phát triển. |
"Còn việc có cấp phép khẩn cấp cho vắc xin Nanocovax hay không là quyết định của Hội đồng cấp phép. Hội đồng Đạo đức chỉ là bên đưa ra ý kiến tư vấn", GS Dũng nói khi được hỏi liệu với những dữ liệu này vắc xin của Nanogen đã đủ điều kiện để cấp phép khẩn cấp.
Một thành viên của Hội đồng Tư vấn cấp giấy đăng ký lưu hành thuốc, nguyên liệu làm thuốc của Bộ Y tế cũng cho biết hiện Hội đồng chưa có cuộc họp nào về việc cấp phép vắc xin Nanocovax.
Trước đó, trong 3 ngày 20-22/8, Hội đồng Đạo đức đã họp, thẩm định báo cáo giữa kỳ pha 3a vắc xin Nanocovax, đánh giá về tính an toàn và tính sinh miễn dịch của vắc xin.
Theo nhóm nghiên cứu vắc xin Nanocovax đạt yêu cầu về tính an toàn và tính sinh miễn dịch. Gộp chung giai đoạn 2 và 3a, nhóm nghiên cứu kết luận, trung bình nhân nồng độ kháng thể Anti-S-IgG đạt 57.56 U/ml, tăng gấp 218,93 lần sau 42 ngày tiêm vắc xin. Tỷ lệ chuyển đổi huyết thanh đạt 99,2%.
Về các phản ứng phụ sau tiêm như đau tại vị trí tiêm, mệt mỏi, đau khớp, buồn nôn... chủ yếu ở mức độ nhẹ và trung bình. Chẳng hạn, dữ liệu từ 856 người tiêm mũi một và 824 người tiêm mũi 2 cho thấy, có một trường hợp đau nặng tại chỗ tiêm (chiếm 0,1%), tỷ lệ đau nhẹ sau tiêm mũi một và mũi 2 lần lượt là 38,7% và 44,7%, tỷ lệ này ở giả dược dao động 37-42%.
Tỷ lệ bị sốt nhẹ sau tiêm dao động 2,3-3,7%, 0,2% sốt trung bình, 0,1% sốt nặng. Ở nhóm giả dược, nhóm sốt nhẹ dao động từ 1,4-4,8%.
Khoảng 20-25% tình nguyện viên bị mệt mỏi mức độ nhẹ sau tiêm vắc xin, tỷ lệ này ở nhóm giả dược từ 23-29%; mệt mỏi mức độ trung bình dao động 1,2-1,9%, ở nhóm giả dược là 0,7-2,9%.
Ngoài ra, có 29 trường hợp bị tiêu chảy mức độ nhẹ sau tiêm mũi một và 27 trường hợp sau tiêm mũi 2, chiếm tỷ lệ lần lượt 3,4% và 3,3%; 2 trường hợp bị tiêu chảy mức độ trung bình.
Đến thời điểm hiện tại, Nanocovax của Công ty Nanogen là vắc xin Covid-19 đầu tiên của Việt Nam bước sang giai đoạn thử nghiệm lâm sàng thứ 3.
Công ty đang triển khai theo đề cương nghiên cứu. Cụ thể, pha 3 được thử nghiệm trên 13.000 người, chia làm 2 giai đoạn nhỏ (3a: 1.000 người và 3b: 12.000 người). Trong đó, hơn 4.000 tình nguyện viên được tiêm đủ 2 mũi.
Điều kiện để cấp phép khẩn cấp vắc xin Covid-19 sản xuất trong nước
 |
Theo hướng dẫn mới nhất của Bộ Y tế về việc đăng ký lưu hành vắc xin Covid-19 trong trường hợp cấp bách, vắc xin phòng Covid-19 sản xuất trong nước đang thực hiện thử lâm sàng nhưng đã có kết quả đánh giá giữa kỳ giai đoạn 3 về tính an toàn và hiệu quả bảo vệ của vắc xin dựa trên dữ liệu về tính sinh miễn dịch có thể được xem xét cấp phép có điều kiện. Cụ thể sẽ căn cứ trên cơ sở ý kiến tư vấn của Hội đồng đạo đức trong nghiên cứu y sinh học cấp quốc gia (đối với vắc xin thực hiện thử lâm sàng tại Việt Nam) và ý kiến tư vấn của Hội đồng tư vấn cấp giấy đăng ký lưu hành thuốc, nguyên liệu làm thuốc đối với từng vắc xin cụ thể, có tham khảo hướng dẫn hoặc khuyến cáo của Tổ chức Y tế thế giới.
Vắc xin được cấp trong trường hợp trên phải được tiếp tục theo dõi về tính an toàn, hiệu quả, kiểm soát về đối tượng, số lượng, phạm vi sử dụng sau khi cấp giấy đăng ký lưu hành.
Sau khi được cấp phép lưu hành, cơ sở đăng ký phối hợp với cơ sở sản xuất tiếp tục thực hiện nghiên cứu lâm sàng và cập nhật dữ liệu lâm sàng theo hướng dẫn của Bộ Y tế (Cục Khoa học công nghệ và Đào tạo).
Về thủ tục cấp giấy lưu hành vắc xin, trong vòng 20 ngày làm việc kể từ khi nhận được đủ hồ sơ, Cục Quản lý Dược sẽ cấp giấy phép đăng ký lưu hành vắc xin, nếu chưa cấp, Cục sẽ phải thông báo rõ lý do.