Bộ Y tế vào cuộc sau phản ánh của Báo Tuổi trẻ Thủ đô về sản phẩm viên đặt điều trị, dung dịch vệ sinh
Đơn vị phân loại: “Mô tả khả năng se khít âm đạo nhằm tăng tương tác trong quảng cáo”
Như đã nêu ở các bài báo trước, hiện nay trên thị trường tồn tại những loại sản phẩm là viên đặt phụ khoa, kén đặt thảo dược, gel bôi trơn… được quảng cáo là có khả năng thẩm thấu vào bên trong âm đạo nhưng lại được các doanh nghiệp phân loại là mức rủi ro thấp.
Điều bất thường này đã tồn tại trong một thời gian khá dài nhưng không hiểu vì lý do gì các Sở Y tế như Hà Nội, Hà Nam, Bắc Giang... vẫn cấp phiếu tiếp nhận một cách ồ ạt cho các doanh nghiệp.
Thậm chí tại các bản mô tả kỹ thuật của những sản phẩm này còn khẳng định khả năng điều trị, làm se khít, hồng âm đạo… Tuy nhiên, tất cả những công dụng này đều trái với Nghị định 169/2018/NĐ-CP đó là TTBYT không sử dụng cơ chế dược lý, miễn dịch hoặc chuyển hóa trong hoặc trên cơ thể người hoặc nếu có sử dụng các cơ chế này thì chỉ mang tính chất hỗ trợ.
 |
| TTBYT không có tác dụng làm se khít âm đạo nhưng vẫn được đưa vào phần mô tả kỹ thuật nhằm tăng tính quảng cáo |
Trao đổi với phóng viên báo Tuổi trẻ Thủ đô về việc tồn tại những bản phân loại trang thiết bị y tế loại A cho sản phẩm viên đặt phụ khoa như: Viên đặt phụ khoa Nhất Nhất; Viên đặt phụ khoa Thanh cung bảo; viên đặt phụ khoa Hồng quý phi; Kén đặt phụ khoa Kim Nữ; Viên đặt phụ khoa Nữ oa… ông Nguyễn Quốc Đạt, Giám đốc Trung tâm dịch vụ kỹ thuật thiết bị y tế cho biết: “Việc se khít âm đạo là tác động cơ học, khi phân loại tôi cũng yêu cầu các công ty chỉ để mục đích sử dụng đơn thuần thôi nhưng các đơn vị có sản phẩm vẫn mô tả tác dụng se khít, làm hồng của viên đặt âm đạo và họ xin để như vậy chỉ là để tăng tính quảng cáo. Sau khi nhận phản ánh của quý báo, chúng tôi sẽ yêu cầu các Công ty mô tả không đúng mục đích và chỉ định phải sửa hoặc thu hồi...”
Còn ông Lê Đức Hà, Phó Giám đốc Công ty TNHH Khoa học kỹ thuật và thiết bị y tế Đức Phúc, một đơn vị cũng có những bản phân loại bất thường với các sản phẩm Viên đặt phụ khoa Regamo, Viên đặt phụ khoa họ Đinh… lại tỏ ra bức xúc khi bị báo chí phản ánh và cho rằng việc phân loại chưa đúng không làm ảnh hưởng gì đến người tiêu dùng và cho biết người này làm ở Bộ Y tế nên Nghị Định 36 và 169 cũng tham gia xây dựng(?)
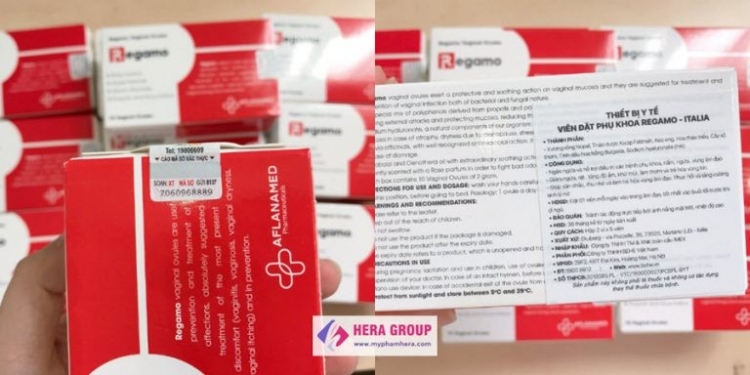 |
| Sản phẩm Regamo được quảng cáo rầm rộ công dụng điều trị viêm nhiễm |
“Chất lượng là do họ công bố, người phân loại không thể kiểm soát được chất lượng, tôi làm bên Bộ Y tế… và tại sao 100 công ty làm viên đặt nhưng lại chỉ đưa Công ty tôi lên...” - ông Lê Đức Hà nói thêm.
Việc cấp phiếu tiếp nhận TTBYT của các Sở Y tế một phần dựa vào kết quả phân loại của những doanh nghiệp được cấp phép làm phân loại nhưng thực tế cho thấy vẫn còn thiếu sự khách quan, thậm chí là “tiếp tay” cho các sản phẩm dạng kén đặt, viên đặt phụ khoa nhằm “lòe” người tiêu dùng bằng những công dụng trên trời như se khít, làm hồng, điều trị… Có những dạng viên đặt phụ khoa như Hồng âm Lan chi X2; Viên đặt Nữ Oa… từng được đăng ký là mỹ phẩm, thực phẩm chức năng nhưng khi bị dư luận phanh phui thì sản phẩm này lại được “lột xác” là TTBYT.
Động thái quyết liệt của Vụ trang thiết bị và công trình Y tế
Sau nhiều lần báo Tuổi trẻ Thủ đô phản ánh và đóng góp ý kiến đến Vụ trang thiết bị và công trình Y tế (Bộ Y tế), mới đây đơn vị này đã ban hành công văn số 3453/BYT-TB-CT gửi đến Sở Y tế các tỉnh, thành phố đề nghị triển khai rà soát, kiểm tra các hồ sơ công bố, tiếp nhận công bố và phân loại trang thiết bị y tế.
 |
| Sản phẩm này từng được Công ty đông y Lan Chi công bố là thực phẩm chắc năng nhưng sau này "lột xác" thành TTBYT loại A |
Trong công văn có nội dung như sau: Để thực hiện đúng các quy định của Nghị định đối với các thủ tục công bố được triển khai tại các Sở Y tế và tăng cường công tác hậu kiểm, rà soát việc tiếp nhận hồ sơ công bố để kịp thời chấn chỉnh, xử lý các trường hợp vi phạm (nếu có) theo quy định của pháp luật, Bộ Y tế đề nghị các Sở Y tế, rà soát, kiểm tra các hồ sơ công bố tiêu chuẩn áp dụng đối với trang thiết bị y tế loại A (hồ sơ công bố sản phẩm) thực hiện không đúng quy định của Nghị định đối với các trường hợp, hồ sơ công bố sản phẩm mà thành phần hồ sơ chưa đầy đủ, không đúng quy định, không công bố đủ điều kiện sản xuất nhưng đã công bố tiêu chuẩn áp dụng đối với trang thiết bị y tế loại A sản xuất trong nước, không có giấy chứng nhận lưu hành tự do đối với trang thiết bị y tế loại A nhập khẩu, văn bằng chứng chỉ người chịu trách nhiệm chuyên môn không đúng quy định của Nghị định, không có nhãn, hướng dẫn sử dụng,...
 |
| Nhìn bên ngoài sản phẩm ai cũng ngỡ là dang viên đặt nhưng thực chất bên trong vỉ là dạng kén thảo dược |
Ngoài ra công văn cũng chỉ đích danh những hồ sơ công bố sản phẩm không phù hợp là trang thiết bị y tế như: Gel rửa tay khô, cồn ethanol sát khuẩn vết thương, Povidine Iodine (Cồn Iốt), Oxy già, tinh dầu, dầu gió, bột ngâm chân, viên ngậm, viên đặt điều trị, kem bôi da, dung dịch vệ sinh, dung dịch xua đuổi côn trùng, miếng dán say xe, máy sắc thuốc, các sản phẩm nguồn gốc thuốc y học cổ truyền, dược phẩm, mỹ phẩm, thực phẩm…
Các hồ sơ công bố sản phẩm có phân loại sản phẩm không đúng là TTBYT loại A như Que thử xét nghiệm các chất ma túy; Kim tiêm, kim luồn tĩnh mạch; Hóa chất xét nghiệm sinh hóa, miễn dịch, huyết học; Que thử thai, rụng trứng, HIV.
Việc rà soát, thu hồi giấy công bố TTBYT loại A của các Sở Y tế sẽ tiến hành như thế nào, báo Tuổi trẻ Thủ đô sẻ tiếp tục cập nhập!