Bản tin 115: Phát hiện 2 loại kẹo có chứa chất trị rối loạn cương dương
 |
Phát hiện 2 loại kẹo có chứa chất trị rối loạn cương dương
Ngày 7/3, Cục An toàn thực phẩm (Bộ Y tế) đưa ra thông báo cho biết Phòng thí nghiệm của Cơ quan Khoa học Y tế Singapore (HSA) đã phát hiện 2 sản phẩm "Hickel" và "Solomon Island - Soloco Traditional Candy" (gọi tắt là Soloco) được bán online có chứa hàm lượng cao tadalafil. Đây là một thành phần dược chất không được kê khai trên nhãn sản phẩm vốn được sử dụng để điều trị chứng rối loạn cương dương. Theo HSA, hàm lượng tadalafil trong hai sản phẩm trên cao gấp 30 lần so với liều dùng hằng ngày cho phép. Khi sử dụng hàm lượng cao tadalafil như vậy rất nguy hiểm và có thể gây tăng nguy cơ đau tim, đột quỵ, mất thị giác và thính giác.
Thế nhưng, trên các trang thương mại điện tử, trong đó có facebook, hai sản phẩm trên được quảng cáo là kẹo, có tác dụng cải thiện chức năng tim mạch, thận, hỗ trợ điều trị tiểu đường, tăng cường sinh lực, tăng sức đề kháng và cải thiện chức năng sinh sản.
Cục An toàn thực phẩm đã tiến hành rà soát và kết quả hai sản phẩm trên chưa được cấp công bố nhập khẩu vào Việt Nam. Cục An toàn thực phẩm cũng đã có công văn gửi các cơ quan hải quan và cơ quan kiểm tra nhà nước về an toàn thực phẩm để thực hiện phương thức kiểm tra chặt đối với các sản phẩm nêu trên và yêu cầu 63 Chi cục An toàn vệ sinh thực phẩm trong cả nước tiến hành giám sát các sản phẩm này trên thị trường.
Cục An toàn thực phẩm khuyến cáo người tiêu dùng tuyệt đối không sử dụng các sản phẩm có tên nêu trên và báo với cơ quan chức năng gần nhất nếu phát hiện tổ chức, cá nhân có bán các sản phẩm này.
Bộ trưởng Bộ Y tế yêu cầu cả nước mạnh tay ngăn dịch sởi
Trong năm 2018 và đầu năm 2019, tình hình dịch bệnh sởi diễn biến phức tạp, gia tăng tại nhiều quốc gia, trong đó xảy ra ở một số nước đã công bố loại trừ bệnh sởi. Đặc biệt tại Philippines trong năm 2019 đã ghi nhận 12.736 trường hợp mắc sởi và 203 trường hợp tử vong. Tại Việt Nam, bệnh sởi bắt đầu gia tăng từ tháng 10 năm 2018, tính đến nay ghi nhận 18.078 trường hợp sốt phát ban nghi sởi, trong đó 2.924 trường hợp mắc sởi dương tính được xác định tại 56 tỉnh, thành phố, hiện số mắc vẫn chưa có xu hướng giảm.
Các trường hợp mắc bệnh tập trung chủ yếu tại vùng núi, vùng sâu, vùng xa, vùng dân tộc thiểu số sinh sống và tại các tỉnh, thành phố có nhiều khu công nghiệp, mật độ dân cư cao, giao lưu đi lại lớn. Nguyên nhân chủ yếu là do tiêm vaccine phòng bệnh sởi chưa được thực hiện đầy đủ cùng với chu kỳ bùng phát bệnh sởi thường xảy ra sau 4 đến 5 năm.
Để chủ động ngăn chặn không để dịch bệnh sởi lan rộng, bùng phát mạnh, Bộ trưởng Bộ Y tế yêu cầu Giám đốc Sở Y tế các tỉnh, thành phố trực thuộc Trung ương chủ trì chỉ đạo tập trung thực hiện những nhiệm vụ trọng tâm tham mưu với UBND tỉnh, thành phố chỉ đạo chính quyền các cấp huy động lực lượng phối hợp với y tế địa phương thống kê đối tượng trong độ tuổi tiêm chủng (tiêm chủng thường xuyên và tiêm chủng chiến dịch) để triển khai tiêm đủ mũi vaccine phòng sởi cho trẻ đạt tỷ lệ ít nhất 95% theo quy mô xã, phường.
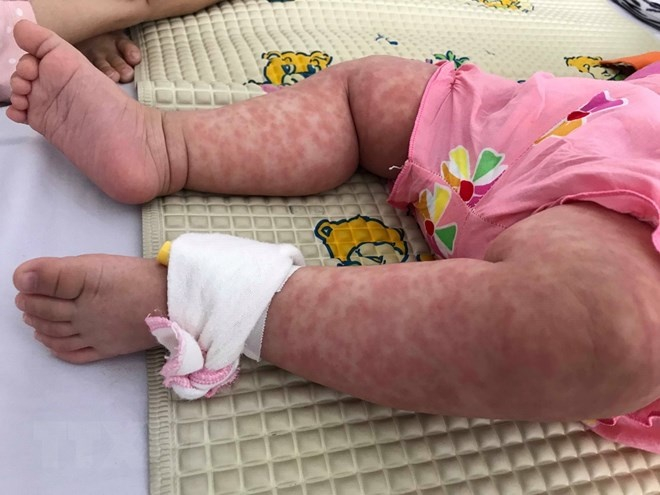
Trẻ mắc sởi đang gia tăng đột biến.
Đảm bảo kinh phí cho các hoạt động tiêm chủng gồm tiêm chủng thường xuyên, tiêm chủng chiến dịch phòng chống dịch sởi cũng như kinh phí mua tiêm phòng sởi cho các đối tượng nguy cơ cao ngoài độ tuổi thuộc Chương trình tiêm chủng mở rộng.
Người nhiễm HIV nhận thuốc ARV qua bảo hiểm y tế từ ngày 8/3
Ngày 8/3, tại nhiều cơ sở y tế trên cả nước đã đồng loạt diễn ra sự kiện “Những bệnh nhân đầu tiên nhận thuốc ARV từ nguồn bảo hiểm y tế”.
Tiến sĩ Hoàng Đình Cảnh, Phó Cục trưởng Phòng, chống HIV/AIDS, cho biết, ARV là thuốc ức chế sự phát triển của virus HIV trong cơ thể người bệnh. Thuốc ARV đã triển khai tại Việt Nam hơn 10 năm nay từ nguồn tài trợ quốc tế, cấp miễn phí cho người nhiễm HIV. Hiện hơn 115.000 người nhiễm HIV được điều trị ARV.
Nguồn viện trợ đã kết thúc vào năm 2018, khi Việt Nam thoát khỏi ngưỡng nước nghèo. Chính phủ chủ trương bảo hiểm y tế sẽ chi trả chi phí thuốc ARV cho người nhiễm HIV có thẻ bảo hiểm y tế.
Người nhiễm HIV phải điều trị bằng thuốc ARV liên tục và suốt đời, chi phí rất cao bao gồm thuốc, các xét nghiệm CD4, tải lượng virus, xét nghiệm chức năng gan, thận... Nếu bảo hiểm không chi trả, người bệnh phải tốn kém nhiều và nhiều trường hợp bỏ điều trị.
Theo thống kê của Cục Phòng chống HIV/AIDS, hiện cả nước có 209.000 người nhiễm HIV còn sống. Ngành y tế đang quản lý 175.000 bệnh nhân, còn 45.000 người chưa tiếp cận được với thuốc ARV. Những người này có thể không kiểm soát được tải lượng virus sẽ làm lây lan ra cộng đồng qua các hành vi tình dục hoặc tiêm chích không an toàn.
Thuốc ARV giúp người bệnh khỏe, giảm tử vong, nâng cao tuổi thọ, giảm lây truyền HIV do khống chế lượng virus trong máu người nhiễm giảm ở mức thấp.
Khi tải lượng virus dưới ngưỡng phát hiện 200 bản sao/ml máu sẽ không lây truyền HIV qua quan hệ tình dục. Phụ nữ mang thai nhiễm HIV được điều trị ARV sớm thì đến 98% trẻ sinh ra không lây nhiễm.
Đình chỉ lưu hành thuốc viên nén Sebemin
Sáng 8/3, Sở Y tế TPHCM cho biết đã có văn bản gửi các cơ sở khám chữa bệnh, các cơ sở kinh doanh thuốc, trung tâm thương mại dược phẩm và trang thiết bị y tế về việc đình chỉ lưu hành thuốc viên nén Sebemin không đạt chất lượng.
Theo đó, để đảm bảo an toàn cho người sử dụng, Sở Y tế TPHCM yêu cầu các cơ sở kinh doanh thuốc, các cơ sở khám chữa bệnh không được buôn bán, sử dụng thuốc viên nén Sebemin (Betamethason 0,25mg và d-Chlorpheniramin maleat 2mg; SĐK:VN-14320-11; Số lô SDM17110; Ngày sản xuất 24-10-2017) do Công ty Crown Pharm.Co.,Ltd (Hàn Quốc) sản xuất, Công ty cổ phần Dược liệu trung ương 2 (Phytopharma) nhập khẩu.
Lý do: thuốc không đạt tiêu chuẩn về chỉ tiêu độ đồng đều hàm lượng Betamethasone. Sở Y tế TPHCM cũng yêu cầu phòng y tế 24 quận/huyện thông báo đến các cơ sở hành nghề y dược trên địa bàn quản lý; Thanh tra Sở Y tế kiểm tra, giám sát các cơ sở kinh doanh và sử dụng thuốc, xử lý theo quy định đối với cơ sở vi phạm.
Bộ Y tế yêu cầu thu hồi, ngừng sản xuất viên Tiểu đường hoàn
Cơ quan chức năng phát hiện, nguyên liệu sản xuất Tiểu đường hoàn Difoco không đúng với công bố.
Cục An toàn thực phẩm, Bộ Y tế vừa kiểm tra việc sản xuất, lưu hành sản phẩm thực phẩm bảo vệ sức khỏe tiểu đường hoàn của Công ty Cổ phần Difoco. Sản phẩm được giới thiệu 100% từ thảo dược thiên nhiên giúp bệnh nhân tiểu đường ổn định đường huyết.
Đây là sản phẩm do Chi nhánh Công ty Cổ phần Difoco công bố, sản xuất tại địa chỉ Khu phố 6 phường Bình Trị Đông A, quận Bình Tân, TP.HCM.
Qua kiểm tra, cơ quan chức năng phát hiện nguyên liệu sản xuất sản phẩm không đúng với công bố.

Viên tiểu đường DIFOCO bị thu hồi
Cụ thể, sản phẩm tiểu đường hoàn được sản xuất từ nguyên liệu có tên "thảo dược tiểu đường", "thảo dược hỗ trợ tiểu đường" đã phối trộn sẵn, không đúng với tên nguyên liệu đã công bố.
Đáng lưu ý, Chi nhánh Công ty Cổ phần Difoco đã không còn hoạt động tại địa chỉ: 276/17/2 Mã Lò, Khu phố 6, phường Bình Trị Đông A, Bình Tân, TP.HCM, nơi đặt cơ sở sản xuất sản phẩm thực phẩm bảo vệ sức khỏe Tiểu đường hoàn.
Theo đó, Cục đã ban hành văn bản yêu cầu Công ty Cổ phần Difoco ngừng sản xuất, buôn bán, lưu thông trên thị trường sản phẩm thực phẩm bảo vệ sức khỏe Tiểu đường hoàn, đồng thời yêu cầu công ty này thu hồi toàn bộ các lô sản phẩm Tiểu đường hoàn đã sản xuất, lưu hành và báo cáo bằng văn bản số lượng sản phẩm đã sản xuất, đã bán, còn tồn kho và thu hồi được.